对乙酰氨基酚(APAP)过量使用是引发药物性急性肝衰竭的首要原因,而目前临床上仍缺乏治疗效果理想且安全性好的特效解毒药物。人参作为传统名贵中药,其主要活性成分人参皂苷在肝病治疗领域具有较大潜力,但发挥保肝作用的靶点与分子机制尚未被系统阐明。
近日,北京大学-云南白药国际医学研究中心副主任叶敏教授团队在British Journal of Pharmacology杂志发表了题为Ginsenoside Rf protects against acetaminophen-induced liver injury by targeting CCAR2 to activate the SIRT1-FXR signalling pathway的研究论文。该研究首次揭示了人参的特征性成分人参皂苷Rf(Ginsenoside Rf)对APAP诱导的急性肝损伤(AILI)的显著防治作用,发现细胞周期与凋亡调节蛋白2(CCAR2)是其发挥药效的直接靶点,并深入解析了CCAR2-SIRT1-FXR信号轴在AILI发生发展过程中的关键调控机制。

一、人参皂苷Rf在体内、体外显著改善APAP诱导的肝损伤
课题组首先比较了人参、西洋参、三七提取物对AML12肝细胞APAP损伤模型的保护作用,发现人参提取物效果最优,并从中筛选出活性最强的成分人参皂苷Rf。在C57BL/6J小鼠模型中,无论是预给药还是同时给药策略,人参皂苷Rf(20或40 mg/kg)均可剂量依赖性地逆转APAP引发的体重减轻与肝脏指数异常,显著减少肝组织坏死面积,并大幅降低血清中谷丙转氨酶(ALT)、谷草转氨酶(AST)及乳酸脱氢酶(LDH)水平。人参皂苷Rf的体内外保肝药效不仅优于文献报道的人参皂苷Rg1,也优于目前临床唯一获批的阳性解毒剂N-乙酰半胱氨酸(NAC)(图1)。
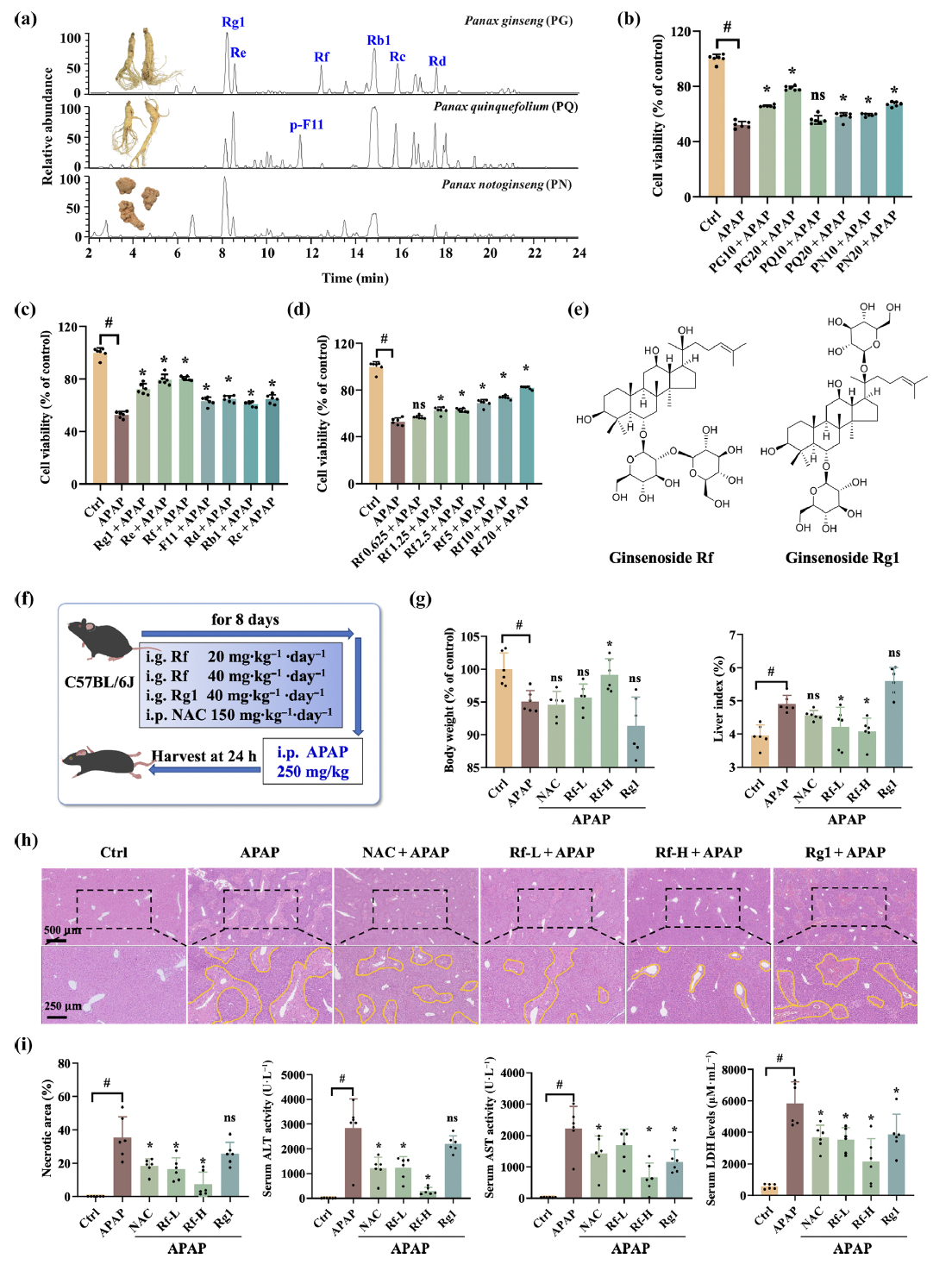
图1 人参皂苷Rf在体内、体外对APAP诱发肝损伤的保护作用。
二、人参皂苷Rf有效抑制APAP诱导的氧化应激、炎症反应与肝细胞凋亡
氧化应激与炎症反应是APAP诱发肝细胞坏死的关键驱动因素。研究表明,人参皂苷Rf干预能显著改善受损肝脏的氧化应激状态,降低丙二醛(MDA)水平,回补谷胱甘肽(GSH)储量并恢复超氧化物歧化酶(SOD)活性;同时显著下调促炎因子(如Il-1β、Tnf-α)的转录水平。此外,TUNEL染色与免疫印迹结果证实,人参皂苷Rf有效清除了肝细胞内蓄积的活性氧(ROS),并降低BAX/BCL2蛋白表达比值,阻断了APAP诱导的肝细胞凋亡进程(图2)。
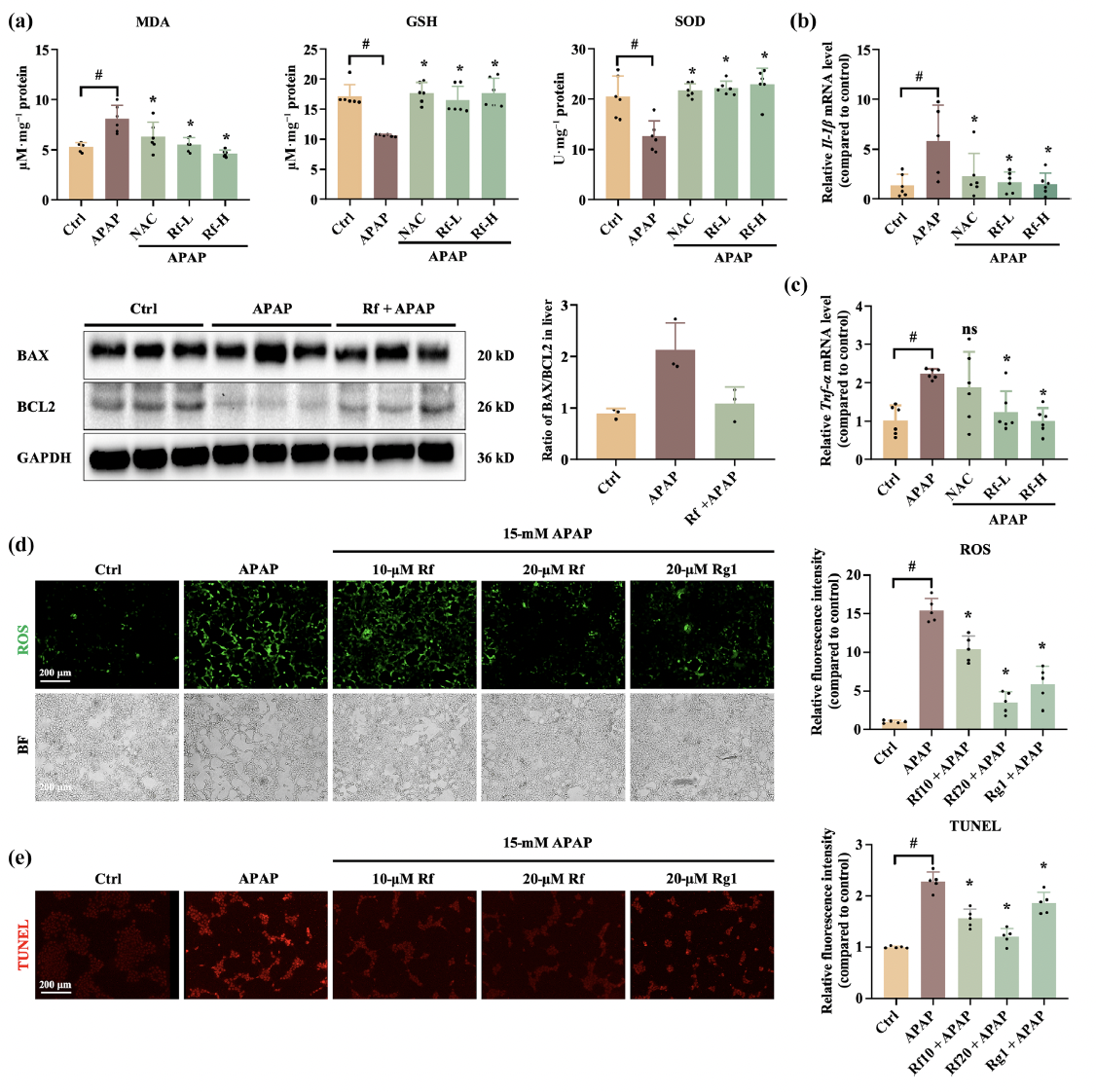
图2 人参皂苷Rf在体内外抑制氧化应激、炎症反应与细胞凋亡。
三、利用蛋白质谱等技术确证CCAR2是Rf的直接结合靶点
为了探寻人参皂苷Rf的直接作用靶点,研究人员设计合成了Rf交联的环氧基磁珠,从小鼠肝脏蛋白裂解液中进行Pull-down垂钓。综合LC-MS/MS蛋白质组学分析、药物亲和反应靶标稳定性(DARTS)、细胞热位移分析(CETSA)及微量热泳动(MST,Kd=5.93 μM)等多重靶点确证手段,最终发现并验证了细胞周期与凋亡调节蛋白2(CCAR2)是人参皂苷Rf的直接结合靶蛋白。分子对接模拟进一步显示,人参皂苷Rf能够与CCAR2的特定氨基酸残基(Ile522、Val523、Ser249)形成氢键(图3)。此外,在细胞水平敲低CCAR2表达后,人参皂苷Rf对APAP诱导的肝细胞死亡和凋亡的抑制作用显著减弱。上述结果提示,CCAR2可能是人参皂苷Rf发挥肝保护作用的关键靶蛋白。
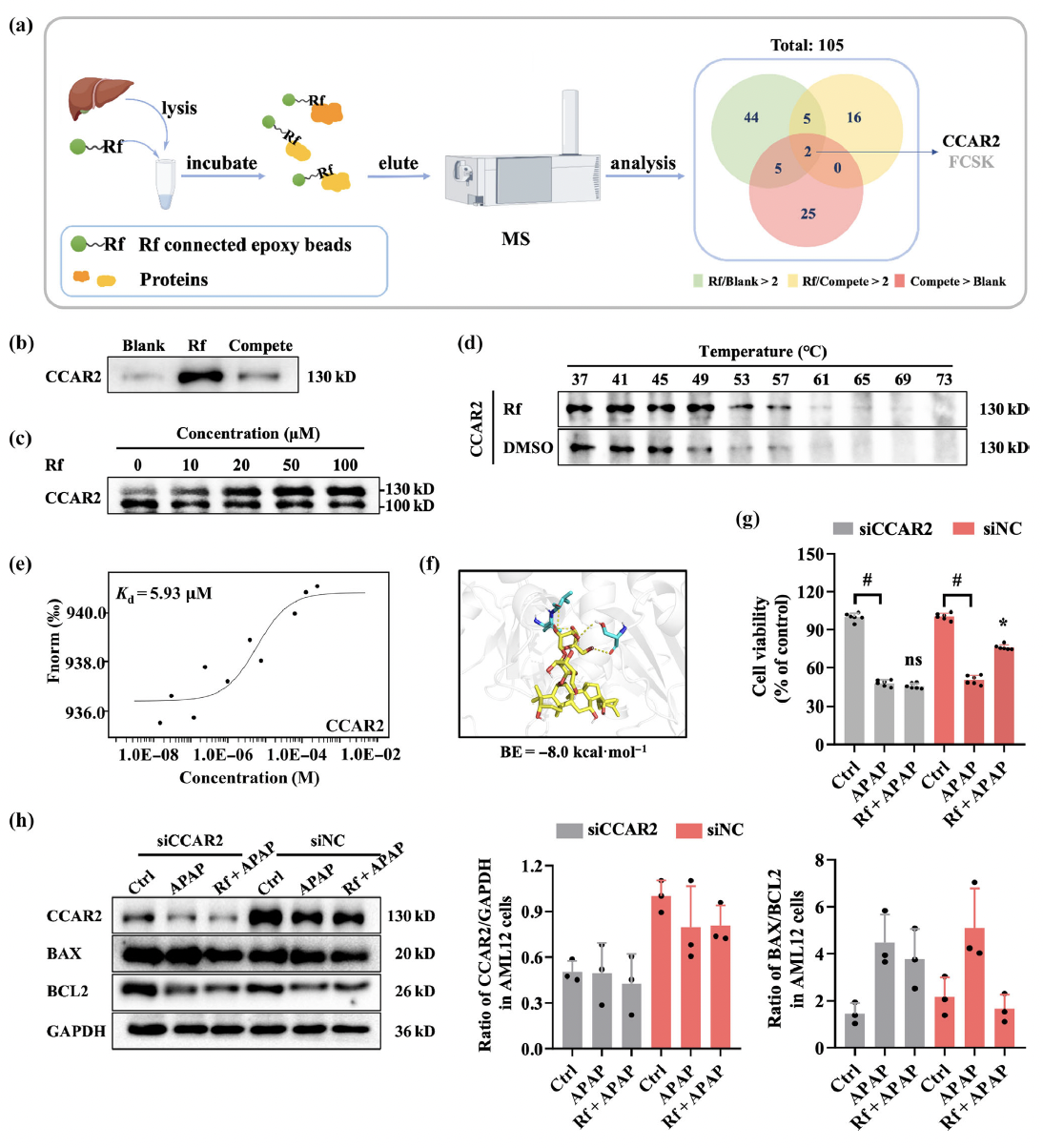
图3 人参皂苷Rf可以与靶蛋白CCAR2直接结合。
四、人参皂苷Rf有效逆转肝脏胆汁酸代谢紊乱
转录组学(RNA-seq)KEGG富集分析与靶向代谢组学(UPLC-MS/MS)分析结果表明,APAP过量导致小鼠胆汁酸代谢通路基因表达水平和胆汁酸谱的紊乱,而人参皂苷Rf干预显著改善了这一代谢异常。上述结果表明,重塑胆汁酸代谢稳态是人参皂苷Rf发挥保肝活性的重要环节(图4)。
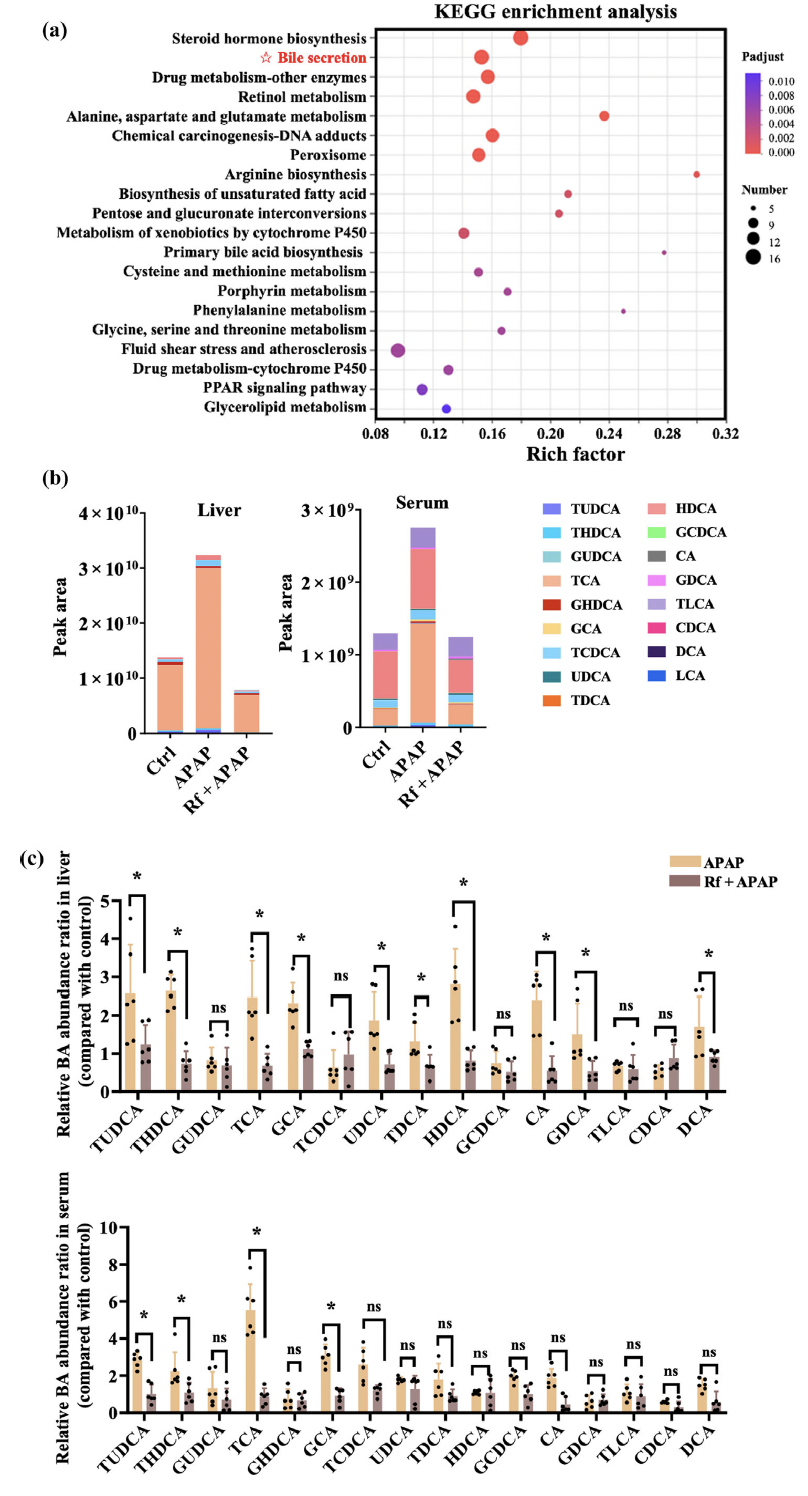
图4 人参皂苷Rf对AILI小鼠肝脏及血清胆汁酸谱的代谢调节。
五、人参皂苷Rf阻断CCAR2-SIRT1相互作用并激活下游FXR信号轴
转录组数据分析及生化实验结果表明,法尼醇X受体(FXR,编码基因为Nr1h4)在人参皂苷Rf的保肝网络中发挥核心调控作用。鉴于CCAR2是沉默信息调节因子1(SIRT1)的内源性抑制蛋白,研究团队推测Rf通过结合CCAR2释放SIRT1。免疫共沉淀(Co-IP)与多重免疫组化(mIHC)实验证明,APAP会诱导CCAR2与SIRT1结合,而人参皂苷Rf通过竞争性结合CCAR2,减少其与SIRT1的相互作用。释放的游离SIRT1进而降低了胞内FXR的乙酰化水平,提高了FXR的蛋白稳定性,促使其更多地穿梭入核。入核转位增加的FXR最终启动了下游胆汁酸转运、抗炎及抗氧化相关靶基因(如Shp、Bsep、Ntcp)的转录表达(图5)。
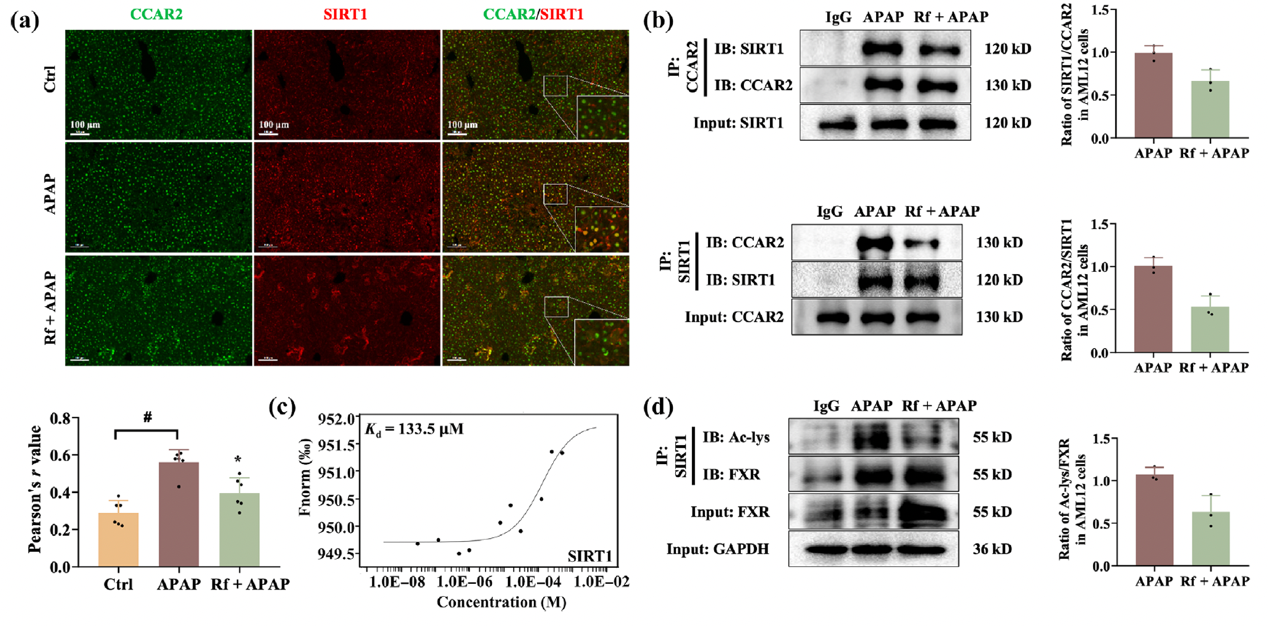
图5 人参皂苷Rf通过阻断CCAR2-SIRT1结合,激活FXR信号通路。
六、肝脏特异性敲低CCAR2反向验证其关键靶点作用
为了在动物水平进一步验证靶蛋白CCAR2的功能,研究人员通过尾静脉注射AAV8病毒包载的sh-CCAR2质粒,构建了肝脏特异性CCAR2敲低(CCAR2-KD)的C57BL/6小鼠模型。敲低CCAR2后,人参皂苷Rf对APAP小鼠的体重维持、肝功能改善及组织坏死面积缩小的保护效应被显著削弱。同时,人参皂苷Rf对炎症因子、氧化应激指标的调控及对胆汁酸稳态的恢复作用也在CCAR2敲低模型中基本丧失(图6)。上述结果表明,人参皂苷Rf通过直接靶向CCAR2发挥治疗AILI的作用。
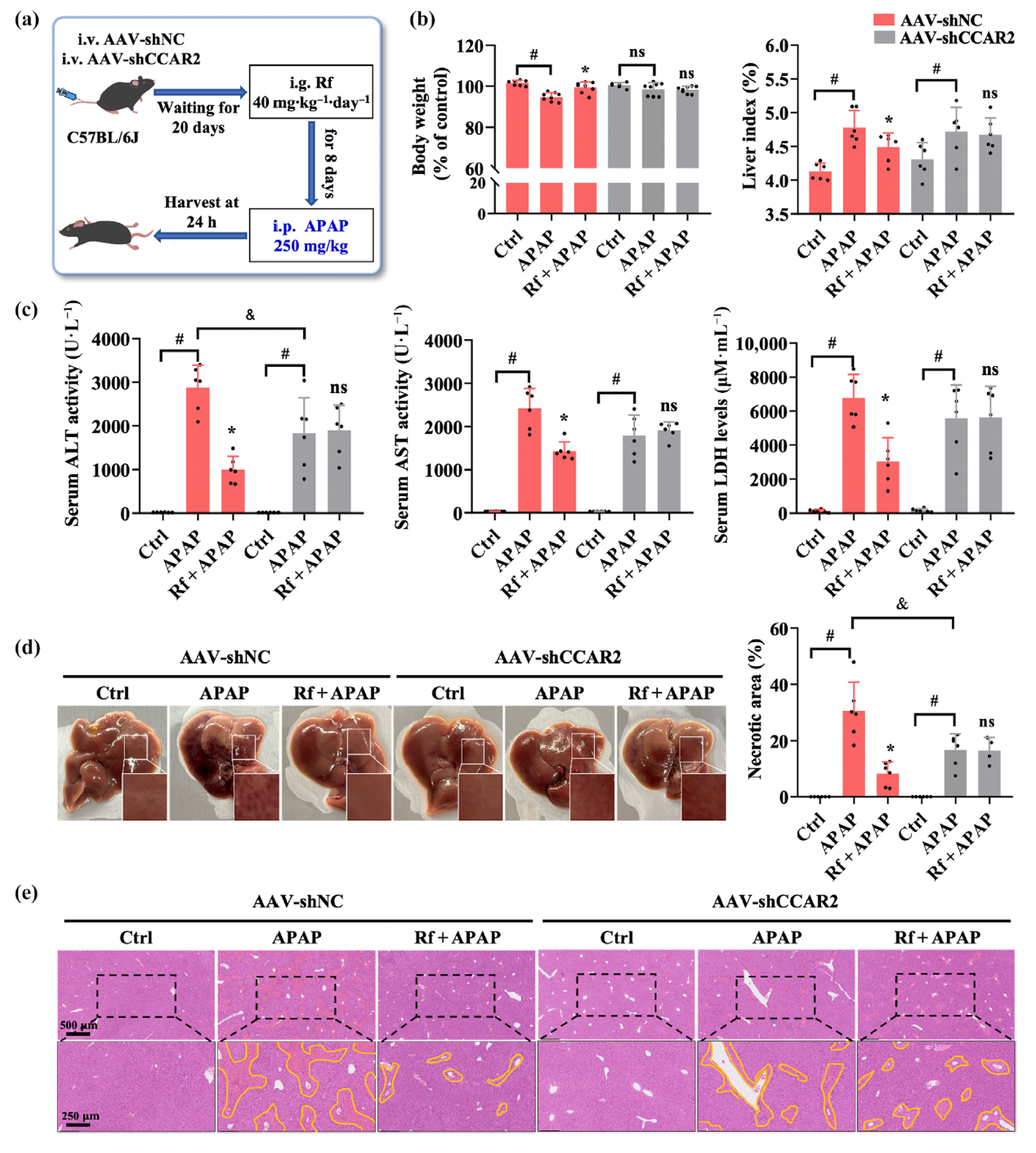
图6 CCAR2敲低显著减弱人参皂苷Rf对模型小鼠的肝脏保护及代谢调节作用。
研究总结
综上所述,该研究发现人参皂苷Rf对APAP导致的肝损伤具有显著的预防和治疗作用。在分子机制层面,人参皂苷Rf通过直接结合CCAR2,阻碍其与SIRT1的相互作用,激活SIRT1-FXR通路,发挥抗氧化、抗炎、抗细胞凋亡及重塑胆汁酸代谢稳态的综合作用。该研究展现了人参皂苷Rf对于药物性肝损伤的应用潜力,并提示CCAR2可能是一个潜在的新靶点。
作者简介
北京大学药学院、北京大学-云南白药国际医学研究中心叶敏教授和黄健副教授为该论文的共同通讯作者,博士研究生范婧婧和六年制学生张清云为共同第一作者。乔雪研究员,余四旺副教授,以及田云刚、张扬、吴若钒等研究生对该研究有重要贡献。该研究得到中央本级重大增减支项目“名贵中药资源可持续利用能力建设项目”(2060302)、国家自然科学基金(No. 81891011)及国家重点研发计划(No. 2023YFA0914100)的资助。
原文链接:
https://bpspubs.onlinelibrary.wiley.com/doi/10.1111/bph.70406

叶敏教授团队合影